 2025-09
2025-09一、引言
2023年6月,国家药品监督管理局食品药品审核查验中心发布了《药品共线生产质量风险管理指南》,该指南强调了MAH应该向受托企业提供品种相关的基于健康的暴露限度(Health Based Exposure Limits,HBEL)。而在评价HBEL时,每日允许暴露量(Permitted Daily Exposure,PDE)及每日可接受暴露量(Acceptable Daily Exposure,ADE)是被普遍接受的标准。
相较于1/1000 最低日治疗剂量、10ppm方法等传统方法设定的限度而言,PDE值在评估清洁残留数据时更具有科学性和优势。最近2年来的监管实践中,省局已经开始要求MAH对计算新引入品种的PDE值,对于已有品种也需要更新其PDE值。
二、PDE的计算公式
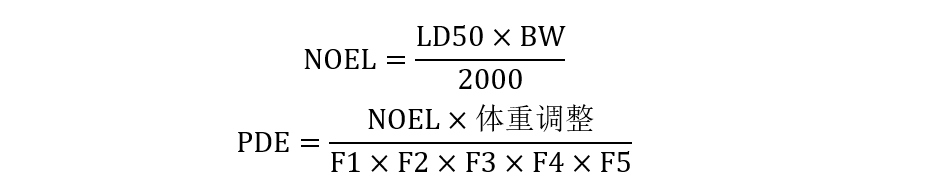
指南中提到的PDE的常用计算公式如下所示:
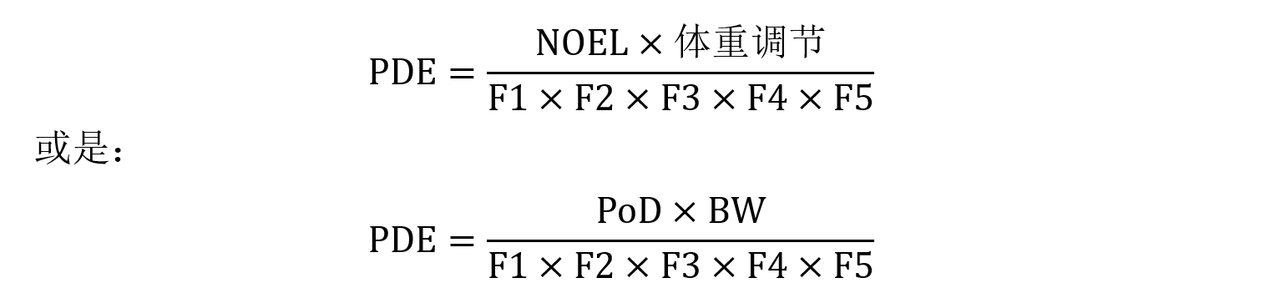
以上公式中的体重调节、BW一般取50kg。因为适用于人类的PDE值,是建立在基于动物试验得到的毒理学数据进行计算的,因此需要引入校正因F1~F5,其大致从物种间差异、个体差异、研究时间、生殖毒性、无作用水平这5个方面进行校正,此处不展开阐述,详情可见ICH《Q3C(R9):杂质:残留溶剂的指导原则》。
起始点(Point of Departure,PoD)是指用于推导PDE的剂量-效应曲线上的起点。PoD是公式2的核心,它涵盖NOEL、NOAEL、LOEL、LOAEL等概念,而NOEL又是公式1的核心,因此后者的适用范围更广。下表列出了NOEL、NOAEL、LOEL、LOAEL的定义及理解。
概念缩略 |
中文名称 |
理解(仅供参考) |
NOEL |
未观察到作用水平 |
在满足“试验动物未出现良性、中性或不良反应”的系列剂量中,最高剂量即为NOEL,剂量继续上调可能会触及LOEL |
NOAEL |
未观察到不良作用水平 |
在满足“试验动物未出现不良反应”的系列剂量中,最高剂量即为NOAEL,剂量继续上调可能会触及LOAEL |
LOEL |
观察到作用的最低水平 |
在满足“试验动物出现良性、中性或不良反应” 的系列剂量中,最高剂量即为LOEL,剂量继续下调可能会触及NOEL |
LOAEL |
观察到不良作用的最低水平 |
在满足“试验动物出现不良反应”的系列剂量中,最高剂量即为LOAEL,剂量继续下调可能会触及NOAEL |
三、PoD的查询
通常,只有原研厂家会充分研究药物的毒理学数据,可查询原研提交于各国药监局的审评报告。
(1)FDA药学审评报告
1、在Drugs@FDA Search的搜索框中输入“Febuxostat”(非布司他)进行搜索。
2、在详情页中选择NDA(新药申请)的品种点开。
![]()
3、点击“Approval Date(s) and History”(批准数据及历史等)一栏中的“review”(审评/审核)。
4、在不同类型的审评文件中,选择“Pharmacology Review(s)”(药学审评文件)。

5、在“TOXICOLOGY”(毒理学)板块即可找到“the no effect dose”(无效应剂量,等同于NOEL)为3mg/kg/d。

(2)EMA公共评价报告
1、在EMA Medicine搜索框中输入“Febuxostat”(非布司他)进行搜索。

2、在结果页中选择上市时间最早的。
3、在详情页中,下拉找到“Assessment history”(评估历史)中的“Initial marketing authorisation documents”(初始上市许可文件)下的“Public assessment report”(公告评价报告)
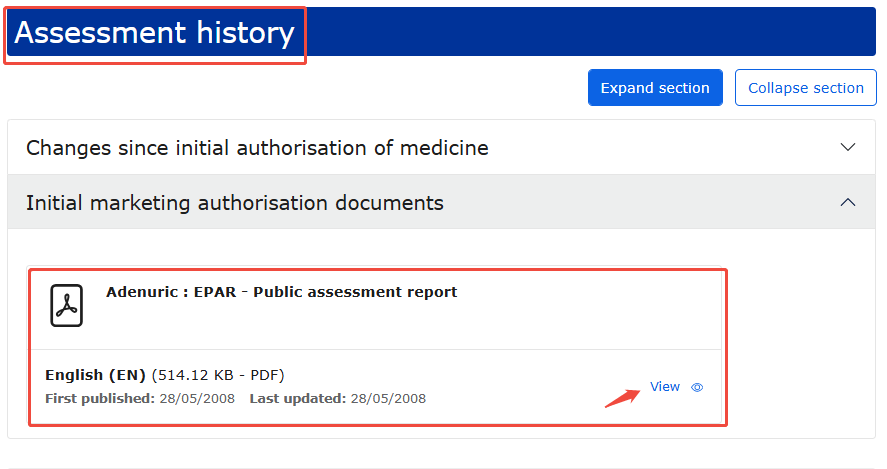
4、报告中的“Toxicology”(毒理学)项下可查询到NOAEL为3mg/kg/d(小鼠)、5mg/kg/d(犬)。需分别代入公式计算PDE,以计算值更小者为准。

(3)PMDA審査報告書
1、在PMDA医療用医薬品 情報検索搜索框中输入“フェブキソスタット”进行检索。
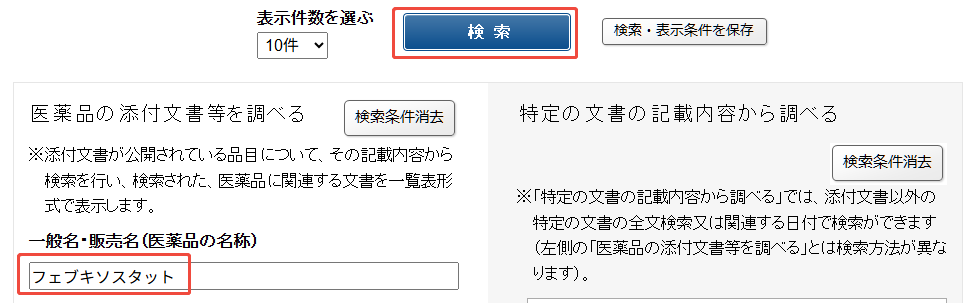
2、翻到结果页的最后一页,在“審査報告書”一列中选择时间最早的审查报告书即可。
3、报告中,在“毒性試験成績の概要”项下可找到“本试验的无毒性量被判断为15mg/kg/日(大鼠,5周)、12mg/kg/日(大鼠,26周)、20mg/kg/日(兔,13周)”等信息,等同于NOEL。需分别代入公式计算PDE,以计算值更小者为准。

(4)其他
当FDA、EMA、PMDA的审评报告均未能查询到PoD,则可尝试以下几种方式:
1)药品说明书:以非布司他片原研在中国地产化的说明书为例,在毒理研究项下,生殖毒性:非布司他经口给药剂量达48mg/kg/d(约为人用剂量80mg/d时血浆暴露量的35倍)时,对雄雌大鼠生育力和生殖行为未见明显影响。
2)化学品安全技术说明书(MSDS):以左炔诺孕酮为例,可在bing(国际版)搜索框内输入“Levonorgestrel MSDS PDF”(药品名称+ MSDS+ PDF),很容易得到其MSDS文件。在这份文件中,一般会有该产品的职业接触限值(OEL)或半数致死量(LD50),这二者均可用于计算PDE值。
①职业接触限值(OEL)

已知左炔诺孕酮的OEL= 0.05µg/m3,按照工人8小时的呼吸量为10m3计算,则左炔诺孕酮的每日最大暴露量PDE=0.5μg/d=0.0005mg/d。
②LD50
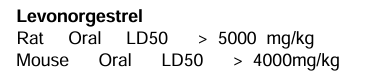
已知左炔诺孕酮的LD50=5000mg/kg(大鼠),根据《GMP指南(口服固体制剂)》(2023版):
公式1中的2000为经验常数。不难看出,使用LD50计算PDE时,“体重”在公式出现了2次(BW、体重调整),此处有重复计算的嫌疑。找到公式1的文献(GUIDANCE ON ASPECTS OF CLEANING VALIDATION IN ACTIVE PHARMACEUTICAL INGREDIENT PLANTS),文中提到“如果没有可用的 NO(A)EL 或 LO(A)EL,LD50 可以用作 PoD”。因此,当仅有LD50毒理学数据可用时,应按照以下公式计算PDE:
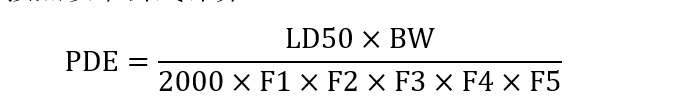
③其他数据库或官网:
四、结语
随着各省药监局在监管过程中逐步落实《药品共线生产质量风险管理指南》, MAH进行生产许可证(A/B/C证)产品增项时,均需在共线生产评估报告中写明PDE的计算及数据来源。本文通过查询FDA、EMA、PMDA的审评报告,或查询其他方式(产品说明书、MSDS、数据库等)等,介绍了几种常见的PDE计算方式,可供各位参考。
五、参考文献
[1] 《药品共线生产质量风险管理指南》
[4] www.pmda.go.jp
[5] 《GMP指南(口服固体制剂)》(2023版)








